- Détails
-
Publication : jeudi 14 avril 2022 16:25
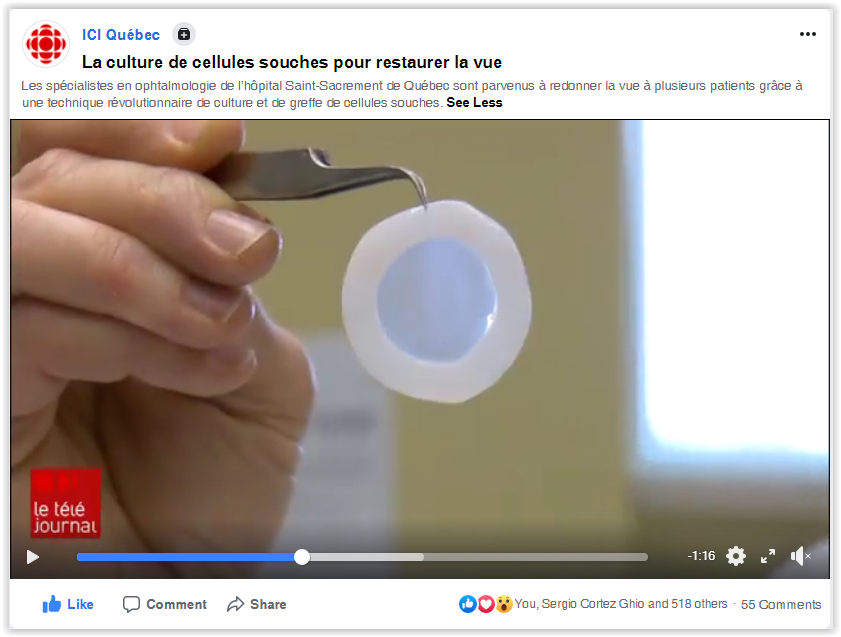
Impact clinique : Perspectives des patients, des chercheurs et des cliniciens sur la transplantation de cellules souches cornéennes.
Entrevue avec M. Damien Bernard, Mme Lucie Germain PhD et Dr René Bazin mené par Julie Fradette, PhD, enregistré durant le congrès Till&McCulloch 2021.
Vidéo en français (with English subtitles) : https://www.youtube.com/watch?v=wGudjHACEV8

- Détails
-
Publication : lundi 12 août 2019 11:27
Un article dans la Presse + du 16 mai 2019 donne des informations concernant «...les cliniques offrant des traitements à base de cellules souches, qui se multiplient au pays - dont plusieurs au Québec. Dans un avertissement publié hier en fin d'après-midi, le ministère fédéral affirme que ces thérapies sont « non autorisées », que leur sécurité et leur efficacité n'ont jamais été prouvées et qu'elles comportent des « risques qui mettent la vie en danger ou altèrent la qualité de vie, comme des infections graves ».
L'article continu en citant un expert dans le domaine: « Plusieurs experts en cellules souches avaient déjà commencé à sonner l'alarme concernant les traitements offerts dans les cliniques privées. C'est le cas de Craig Hasilo, qui est directeur scientifique de CellCAN - un réseau de chercheurs impliqués dans la médecine régénérative et la thérapie cellulaire situé à l'hôpital Maisonneuve-Rosemont.
« Le gros problème avec ces thérapies non prouvées est que la procédure n'a pas été revue par des experts de Santé Canada, avait-il dit à La Presse avant la publication de l'avertissement par Santé Canada. Cela soulève des questions sur ce qui se passe à chaque étape des thérapies et sur les risques à chacune de ces étapes. La sécurité des patients n'a pas été évaluée à chacune des étapes. »
Lire l'article au complet.
Les différentes thérapies sont réglementées sous différents règlements
(Extraits traduits de l’anglais de Cytotherapy, 2017; 19: 1400–1411)
Au Canada, les thérapies cellulaires autologues manipulées de façon minimale à usage homologue sont réglementées soit par la pratique de la médecine, soit comme médicaments ou comme instruments en vertu de la Loi sur les aliments et drogues, du Règlement sur les aliments et drogues ou du Règlement sur les instruments médicaux. Et dernièrement au Canada, la réglementation sur les cellules, les tissus et les organes se limite aux produits allogéniques manipulés de façon minimale à usage homologue. Ceci laisse un vide important dans l'interprétation des réglementations existantes.
L'administration de produits de santé aux patients, y compris les thérapies cellulaires autologues manipulées de façon minimale à usage homologue, est une activité contrôlée considérée comme une pratique de la médecine, qui est auto-réglementée par les médecins au Canada en vertu d'organes légiférés par la province, appelés «collèges».
Les produits de thérapie cellulaire dont la manipulation est plus que minimale, destinés à une utilisation non homologue ou impliquant des actions systémiques ou métaboliques sont généralement réglementés en vertu du Règlement sur les aliments et drogues, car ils répondent tous à la définition de «drogue» au sens de la Loi sur les aliments et drogues. En outre, de nombreuses thérapies cellulaires réglementées en tant que médicaments exigent la présentation d’une demande d’essai clinique avant toute utilisation expérimentale chez l’homme, ainsi que des preuves significatives de la sécurité et de l’efficacité cliniques avant l’autorisation de mise sur le marché. De plus, leur traitement doit être conforme aux exigences GMP.
Cependant, l'application et l'interprétation de ces multiples réglementations demeurent incertaines. Aucune politique n'a été explicitement écrite pour traiter les produits de cellules autologues, manipulés de façon minimale, destiné à un usage homologue et sans effet systémique au Canada.
Note : La majorité des thérapies cellulaires offertes sous forme d’essai clinique dans les centres hospitaliers et universitaires sont des thérapies utilisant des cellules souches qui répondent à la définition de «drogue» mentionnées dans le texte ci-dessus. Ces essais cliniques visent à prouver l’efficacité et l’innocuité de ces nouvelles thérapies en suivant des protocoles d’essai établis scientifiquement et des principes reconnus de l’éthique de la recherche. Ainsi, les patients participants à ces essais cliniques dans les centres hospitaliers et universitaires peuvent accéder de façon éclairée à ces thérapies novatrices dans un contexte bien supervisé.
- Détails
-
Publication : lundi 12 août 2019 11:20
Santé Canada avise les Canadiens contre les risques possibles pour la santé associés aux thérapies cellulaires non autorisées, dont les thérapies à base de cellules souches
Date de début : 15 mai 2019
Type de communication : Mise à jour
Sous-catégorie : Médicaments
Source : Santé Canada
Problème : Renseignements importants en matière d'innocuité
Public : Grand public, Professionnels de la santé
Numéro d’identification : RA-69974
OTTAWA – Santé Canada informe les Canadiens que certaines cliniques et certains professionnels de la santé offrent des thérapies cellulaires non autorisées, comme celles à base de cellules souches, dont les allégations santé ne sont pas fondées, en laissant entendre que ces traitements sont sans danger. Ces pratiques peuvent présenter des risques pour les Canadiens. Les traitements non autorisés (c’est-à-dire que leur innocuité et leur efficacité n’ont pas été prouvées) peuvent comporter des risques qui mettent la vie en danger ou altèrent la qualité de vie, comme des infections graves. C’est pour ces raisons que Santé Canada publié une déclaration de principe qui précise le régime d’emploi autorisé de ces produits.
Lire l'avis sur le site de santé Canada